瑞博奥(广州)生物科技股份有限公司
16 年
手机商铺
- NaN
- 0
- 0
- 2
- 2
推荐产品
技术资料/正文
“肉→白骨”解放军总医院用脂肪细胞“种”出血管化活骨,兼具免疫调控功能
37 人阅读发布时间:2026-01-19 09:21
在骨科临床中,大段骨缺损、骨折不愈合、骨坏死等复杂病症一直是治疗的难点。传统的骨移植方法虽有效,却面临免疫排斥、供体有限、二次创伤等困境。
最近,我国科学家取得突破性进展!脂肪细胞竟能“自组装”成“迷你骨头”?我国团队开发新型骨修复类器官,还能调节免疫!
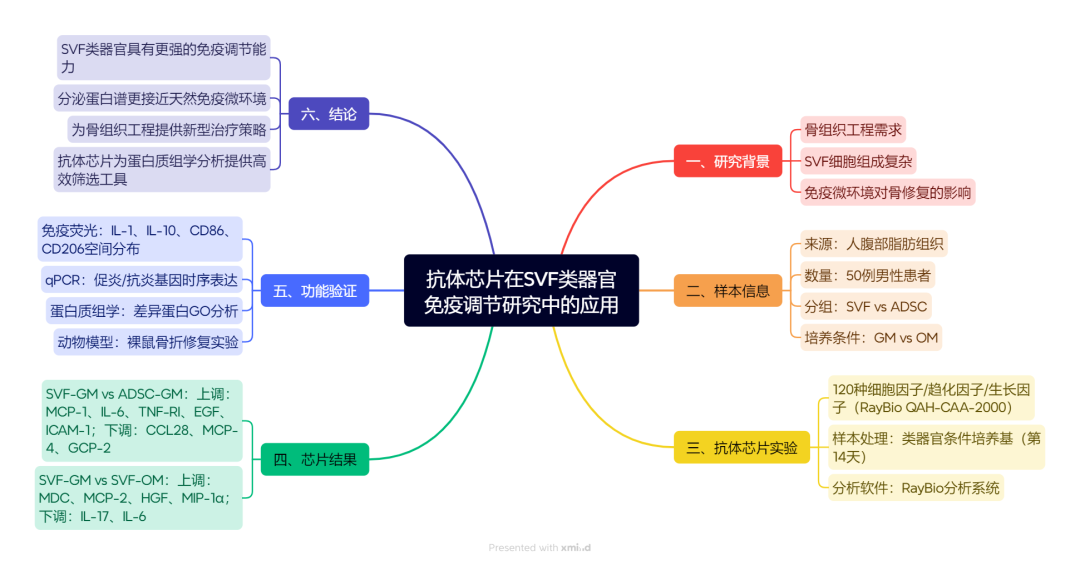
来自中国人民解放军总医院第四医学中心、贵州医科大学等机构的研究团队,创新性地利用脂肪来源的基质血管组分(SVF),成功在体外培育出自组装血管化成骨类器官。这项研究不仅为骨组织工程提供了全新的“活体材料”,更令人惊喜的是,这类器官还展现出强大的免疫调节功能,为复杂骨病的治疗打开了新思路。

杂志名称:Bioact Mater
影响因子:20.3
文章题目:Stromal vascular fraction self-assembles vascularized osteogenic organoids with immunomodulatory functions
第一作者:Jiazhou Wu、Ying He、Tao Qian、Zexian Liu
通讯作者:彭江
作者单位:中国人民解放军总医院第四医学中心骨科研究所;贵州医科大学;锦州医科大学第一附属医院内分泌科等
本实验所用产品:QAH-CAA-2000(检测人类样本中120个炎症、免疫、趋化等微量功能性蛋白)
检测样本:细胞上清
一、研究背景
骨组织工程在治疗大段骨缺损、骨折不愈合和骨坏死等复杂骨科疾病中具有广阔前景。脂肪来源的基质血管组分(SVF)包含多种细胞类型,如间充质干细胞、内皮祖细胞和巨噬细胞,具有成骨、血管生成和免疫调节潜能。本研究旨在利用SVF的自组装能力构建具有血管化、成骨和免疫调节功能的类器官,并与传统脂肪来源间充质干细胞(ADSCs)进行比较,评估其在骨修复中的应用潜力。
二、研究结果
1、SVF与ADSC的细胞组成对比与类器官构建及功能分析
通过流式细胞术分析SVF和P0 ADSCs的细胞组成,发现SVF中含有更高比例的内皮祖细胞(EPCs)、周细胞和免疫细胞(如巨噬细胞),而ADSCs主要为纯化的间充质干细胞。SVF细胞在超低吸附96孔板中经过3天自发聚集成球,形成具有空间组织结构的类器官,而ADSCs则形成致密细胞球体。
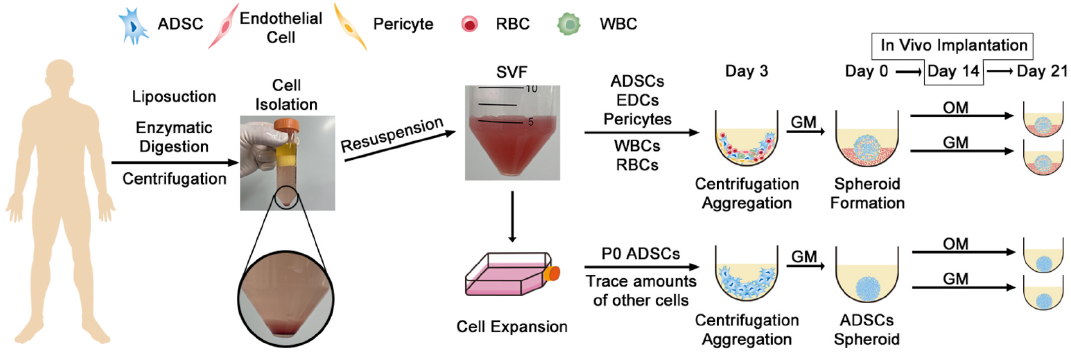
H&E染色、免疫荧光和透射电镜显示,SVF类器官具有更自然的空间组织结构,富含细胞外基质(ECM),并形成血管样网络。相比之下,ADSCs球体结构致密,缺乏血管网络。SVF类器官在生长培养基(GM)中表现出更强的细胞活性和增殖能力,而在成骨诱导培养基(OM)中则出现中心坏死和结构紊乱。
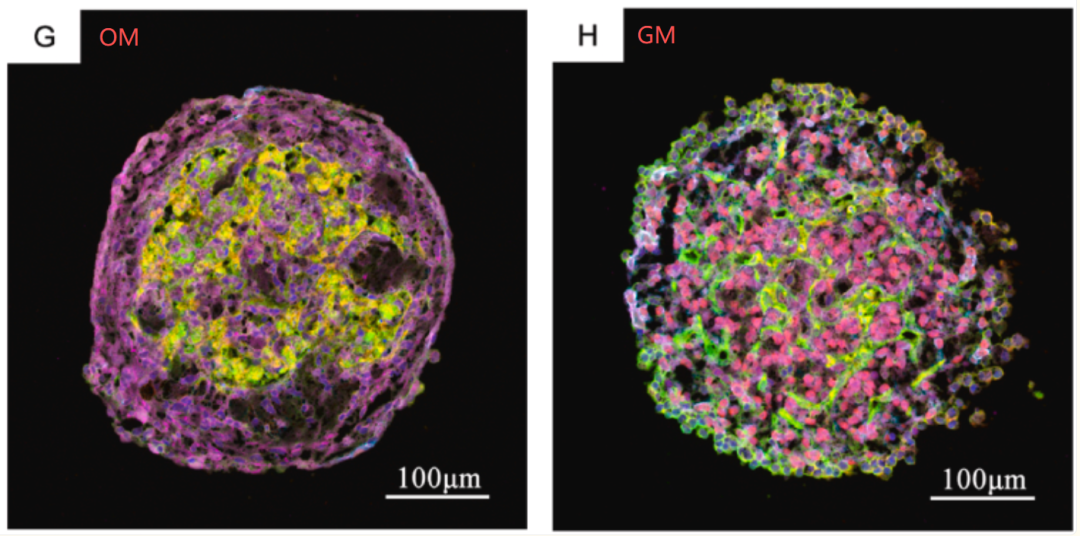
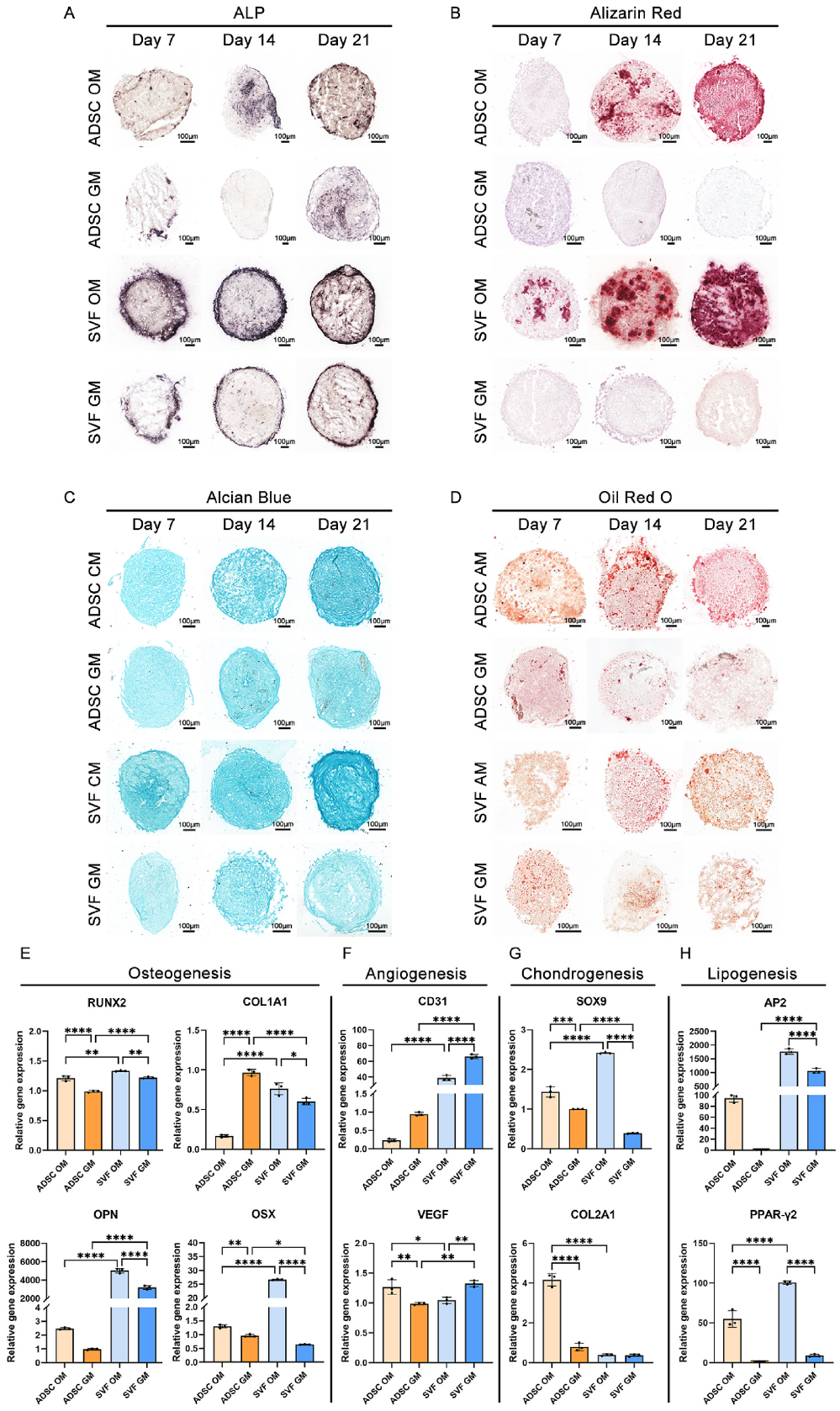
2、SVF类器官多功能分化潜能评估
通过ALP、ARS、ABS和OROS染色以及qPCR分析,发现SVF类器官在成骨、软骨和脂肪分化方面均优于ADSCs。SVF类器官在成骨诱导下表现出更强的矿化和ALP活性,且血管生成相关标志物(CD31、VEGF)表达更高。
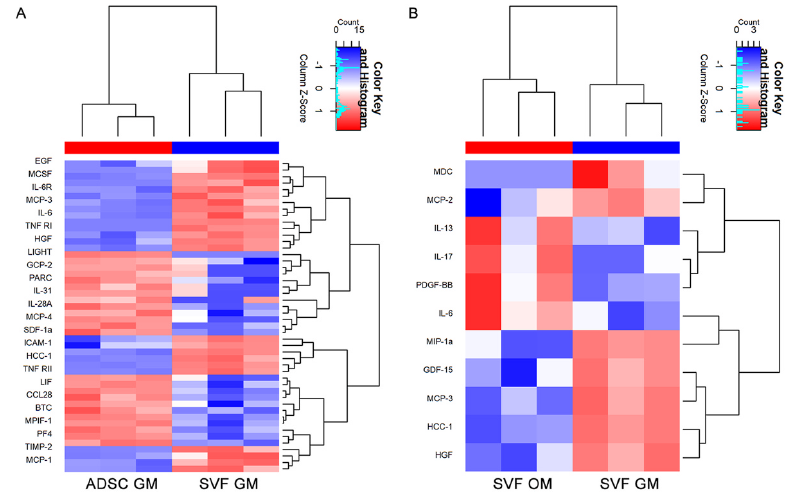
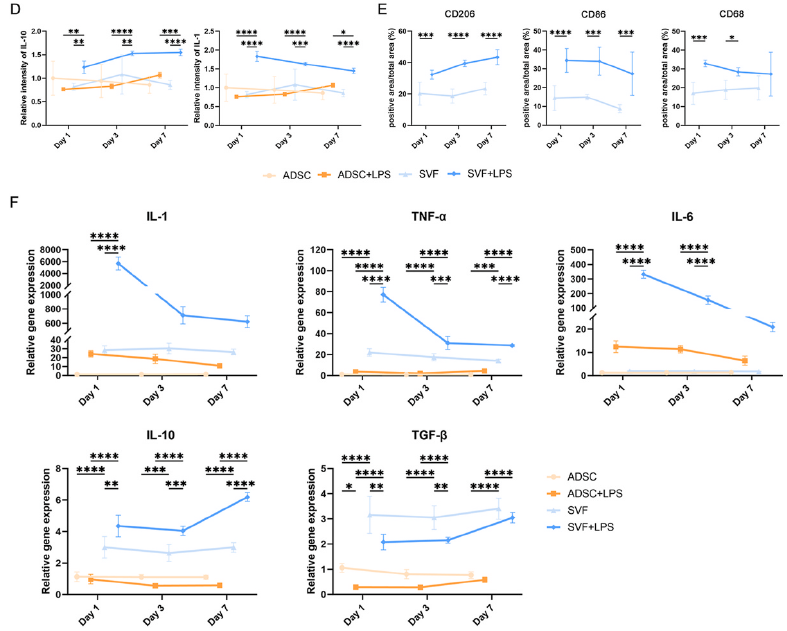
通过蛋白质芯片(RayBio QAH-CAA-2000)和qPCR分析发现,SVF类器官分泌更多与炎症和免疫调节相关的细胞因子(如IL-6、MCP-1、TNF-α等)。在LPS刺激下,SVF类器官表现出更强的免疫调节能力,外周区域表达促炎因子(IL-1),核心区域表达抗炎因子(IL-10),呈现空间依赖性免疫调节模式。
4、SVF类器官体内骨修复效果评估
在裸鼠股骨骨折模型中,植入SVF类器官(尤其是GM组)后,骨折愈合速度更快,骨体积(BV)和骨密度(BMD)显著提高,组织学染色显示更好的骨重塑和血管生成。
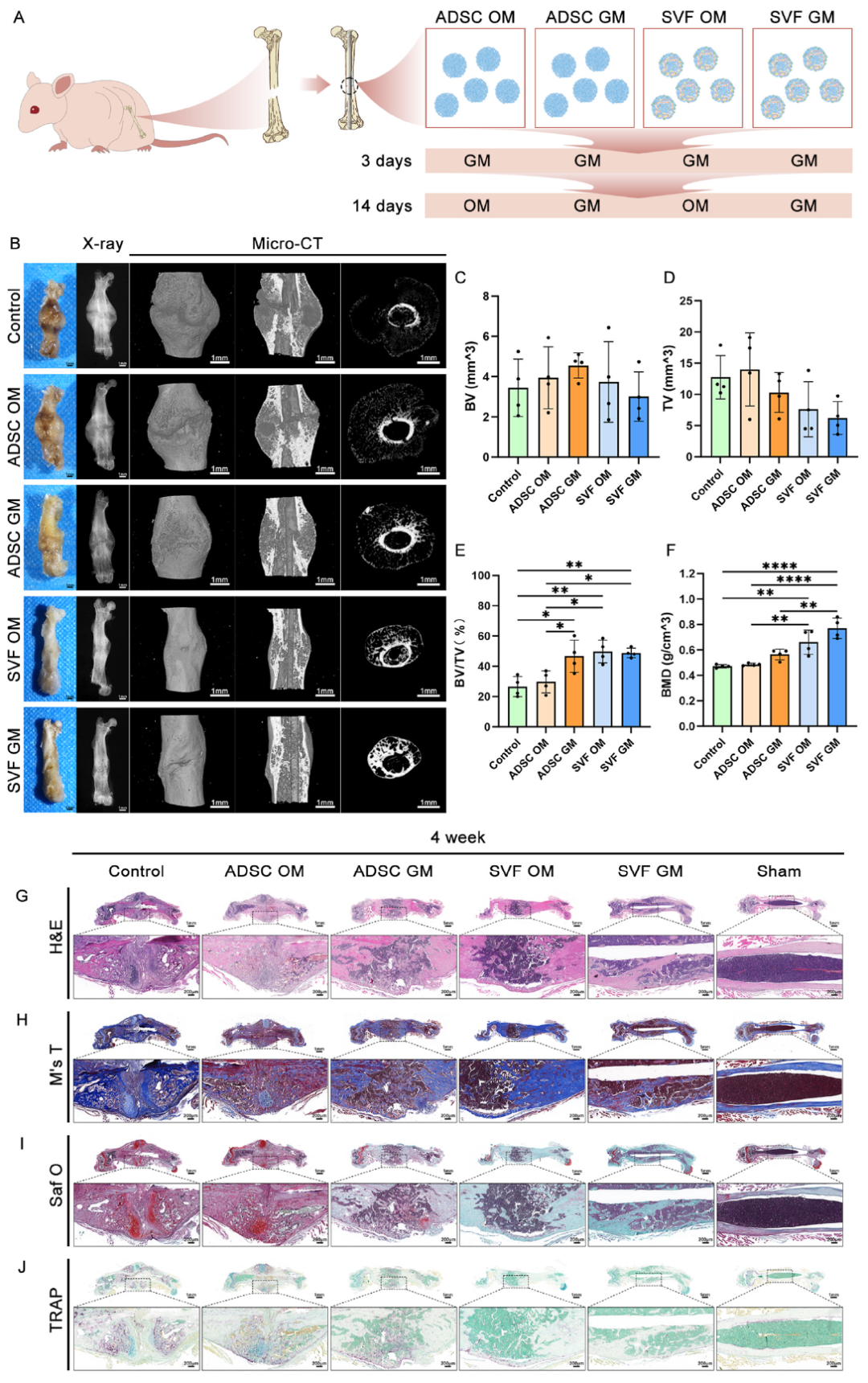
本研究利用SVF成功构建了具有血管化、成骨和免疫调节功能的自组装类器官。与ADSCs相比,SVF类器官在结构复杂度、多功能分化和免疫调节方面均表现更优。体内实验进一步证实其显著促进骨折愈合的能力,且无需预诱导即可发挥骨修复功能。SVF类器官为骨组织工程提供了一种具有临床应用潜力的新型细胞治疗策略。
在研究中为了揭示SVF类器官在免疫调节中的作用,利用了可检测炎症、免疫、趋化、生长等微量功能性细胞多因子抗体芯片,进行SVF类器官免疫调节分泌谱绘制,为“细胞组成-分子分泌-免疫功能”的完整证据链提供了关键数据支撑,是连接表型观察与机制解析的核心技术桥梁。
四、研究结论
本研究利用SVF成功构建了具有血管化、成骨和免疫调节功能的自组装类器官。与ADSCs相比,SVF类器官在结构复杂度、多功能分化和免疫调节方面均表现更优。体内实验进一步证实其显著促进骨折愈合的能力,且无需预诱导即可发挥骨修复功能。SVF类器官为骨组织工程提供了一种具有临床应用潜力的新型细胞治疗策略。
在研究中为了揭示SVF类器官在免疫调节中的作用,利用了可检测炎症、免疫、趋化、生长等微量功能性细胞多因子抗体芯片,进行SVF类器官免疫调节分泌谱绘制,为“细胞组成-分子分泌-免疫功能”的完整证据链提供了关键数据支撑,是连接表型观察与机制解析的核心技术桥梁。