瑞博奥(广州)生物科技股份有限公司
16 年
手机商铺
- NaN
- 0
- 0
- 2
- 2
推荐产品
技术资料/正文
预测贝伐珠单抗疗效:中山大学院士团队早就发现血液标志物组合
106 人阅读发布时间:2026-01-12 16:18
标题: A plasma cytokine and angiogenic factor (CAF) analysis for selection of bevacizumab therapy in patients with metastatic colorectal cancer
杂志: Scientific Reports
研究团队: 中山大学肿瘤防治中心徐瑞华院士团队
一作:白龙,王峰
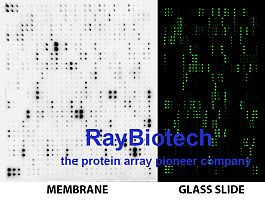
本研究所使用产品: RayBio®Human Angiogenesis Array GS2(货号:GSH-ANG-2,检测人类样本中30种血管生成相关的细胞因子)

实验样品类型: 转移性结直肠癌(mCRC)患者治疗前血浆
一、研究背景
血管生成是结直肠癌发生和进展的关键环节。贝伐珠单抗作为血管内皮生长因子-A(VEGF-A)的单克隆抗体,已成为转移性结直肠癌(mCRC)一线联合化疗的标准治疗方案。然而,其临床疗效存在显著个体差异,部分患者表现出原发性耐药,导致总体生存获益有限。因此,亟需寻找能够精准预测贝伐珠单抗疗效的生物标志物,以实现患者的个体化筛选,从而最大化治疗效益并避免无效治疗带来的毒副作用与经济负担。
二、研究结果
1、通过蛋白质芯片技术筛选出与贝伐珠单抗疗效相关的候选血浆CAFs。
本研究首先利用RayBio®人类血管生成抗体芯片2对64例接受一线贝伐珠单抗联合化疗的mCRC患者(发现队列)的治疗前血浆进行高通量筛查,分析了36种细胞因子和血管生成因子(CAFs)。

通过将蛋白表达水平与患者的无进展生存期(PFS)和总生存期(OS)相关联,初步鉴定出肝细胞生长因子(HGF)、血管内皮生长因子-A121(VEGF-A121)和血管生成素样蛋白4(ANGPTL4)的表达水平与临床结局显著相关。

2、ELISA验证确证了关键CAFs的预测价值。
在包含186例患者(91例接受贝伐珠单抗治疗,95例仅接受化疗)的独立验证队列中,使用ELISA对上述候选标志物进行验证,结果表明:
①低水平HGF或VEGF-A121的患者从贝伐珠单抗治疗中获得的PFS和OS获益显著更大。

②高水平ANGPTL4与贝伐珠单抗治疗后较差的PFS和较低的反应率相关。

③治疗-标志物交互作用检验具有统计学显著性(调整后P交互<0.05),表明这些标志物具有预测价值,而非单纯的预后价值。
3、构建并验证了多标志物联合预测模型(CAF指数)。
为了提升预测能力,研究将ANGPTL4、HGF和VEGF-A121三个标志物整合,构建了一个“CAF指数”。根据各标志物是否低于其最佳截断值进行评分(是=+1,否=0),总分范围为0-3。将患者分为“特征阳性”(评分2-3)和“特征阴性”(评分0-1)。结果显示:
①特征阳性患者从贝伐珠单抗治疗中获得巨大生存获益(中位PFS:11.9 vs. 6.5个月,HR 0.52;中位OS:55.3vs. 28.0个月,HR 0.67)。
②特征阴性患者未能从贝伐珠单抗中获益,OS甚至更差(中位OS:21.1 vs. 29.9个月,HR 1.33)。
③CAF指数与治疗效果的交互作用高度显著(P交互=0.001 for PFS; P交互=0.011 for OS),其预测能力优于任一单一标志物。

研究探讨了结直肠癌发生和进展的潜在生物学机制,利用RayBio® Human Angiogenesis Antibody Array 2这一高通量蛋白筛选技术,无偏倚地快速筛选出与贝伐珠单抗疗效相关的潜在血浆生物标志物谱。
后续讨论了筛选出来的标志物可能的生物学角色:低水平VEGF-A121可能意味着其配体能被贝伐珠单抗更完全地阻断;HGF/c-MET通路的激活可能与对VEGF抑制的抵抗有关;而高水平的ANGPTL4可能代表了一条不依赖于VEGF的、对贝伐珠单抗耐药的替代性血管生成途径。此外,在疾病进展时点观察到HGF和VEGF-A121水平升高,提示它们可能参与了获得性耐药的机制。