瑞博奥(广州)生物科技股份有限公司
16 年
手机商铺
- NaN
- 0
- 0
- 2
- 2
推荐产品
技术资料/正文
IF12.4 细胞外囊泡“运载”Shh信号:南方医科大学团队揭示细胞外囊泡的关键桥梁作用
327 人阅读发布时间:2025-10-13 17:12
杂志名称: Theranostics
影响因子:12.4
文章题目: Extracellular vesicles play a central role in linking podocyte injury to mesangial activation in glomerular disease
第一作者: 刘昭, 刘曦
通讯作者: 刘友华、刘曦
作者单位: 南方医科大学南方医院肾内科,多器官损伤防治国家重点实验室
本研究所实验中所使用的产品:Mouse Cytokine Array G2000(货号:AAM-CYT-G2000,一次性检测小鼠样本中144种细胞因子)

实验样品类型: 小鼠足细胞(MPC5)来源的细胞外囊泡(Ctrl-EVs 与 Ang II-EVs)
研究背景
肾小球疾病的主要特征是蛋白尿和肾小球硬化,分别由足细胞损伤和系膜细胞活化引起。然而,这两个关键事件之间如何联系尚不明确。细胞外囊泡作为细胞间通讯的重要媒介,可能在其中扮演了桥梁角色。声波刺猬因子(Shh)是一种脂修饰信号蛋白,其如何从足细胞传递至系膜细胞是一个未解之谜。本研究旨在探究足细胞来源的EVs是否通过携带Shh来激活系膜细胞,从而连接足细胞损伤与肾小球硬化。
研究结果
1、足细胞损伤与EVs产量增加及Shh富集相关
为模拟肾小球疾病中的足细胞损伤,研究使用血管紧张素II(Ang II)处理小鼠足细胞(MPC5)。结果显示,Ang II在诱导足细胞损伤标志物(ZO-1, Podocalyxin)下调的同时,也显著提高了EVs标志物(TSG101)的表达。透射电镜和纳米颗粒追踪分析证实了从条件培养基中成功分离出EVs。
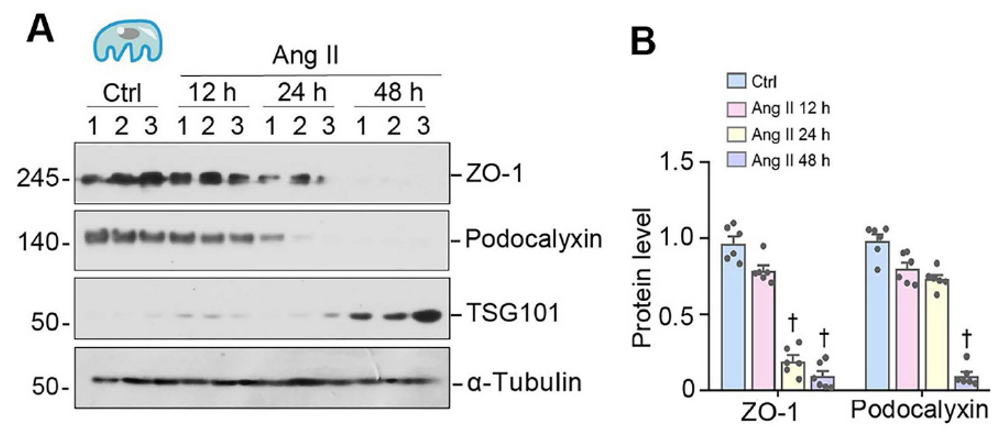
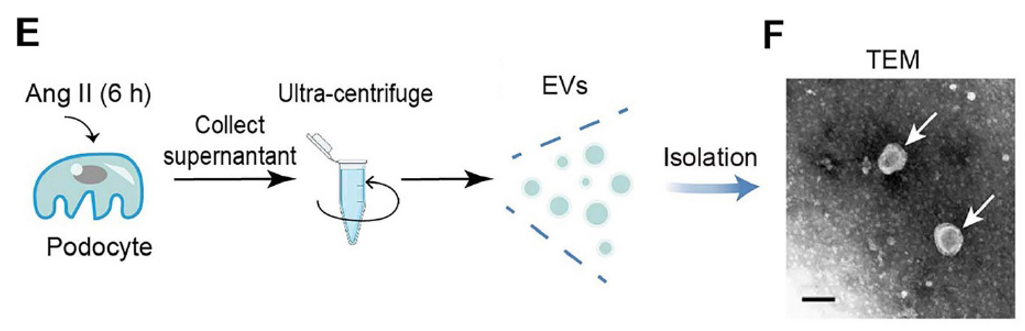
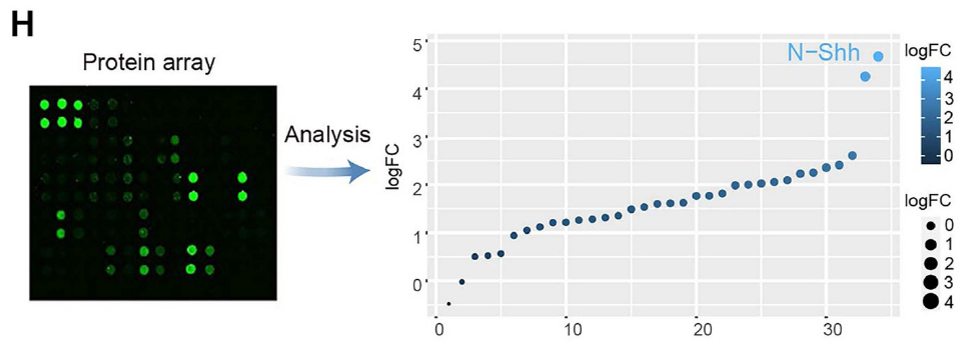
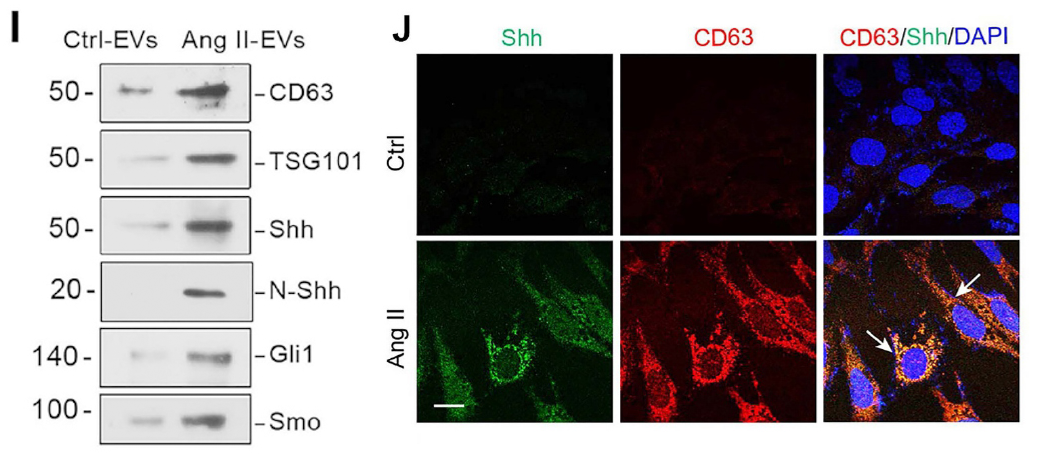
为了揭示介导EVs生物学功能的关键成分,研究采用RayBiotech小鼠细胞因子抗体芯片对来自Ang II处理与未处理足细胞的EVs进行了蛋白质组学分析。芯片结果显示,与对照组EVs相比,N-Shh(Shh的活性形式) 是Ang II-EVs中上调最显著的蛋白。这一关键发现通过Western Blot进一步得到验证,并发现Ang II-EVs中同时封装了Shh信号通路的其他关键成分,如Smo和Gli1。免疫荧光共定位显示,在Ang II处理的足细胞及肾小球疾病模型小鼠和FSGS患者的肾小球中,Shh与EVs标志物CD63存在共定位。
3、抑制足细胞EVs的释放可减轻系膜细胞活化
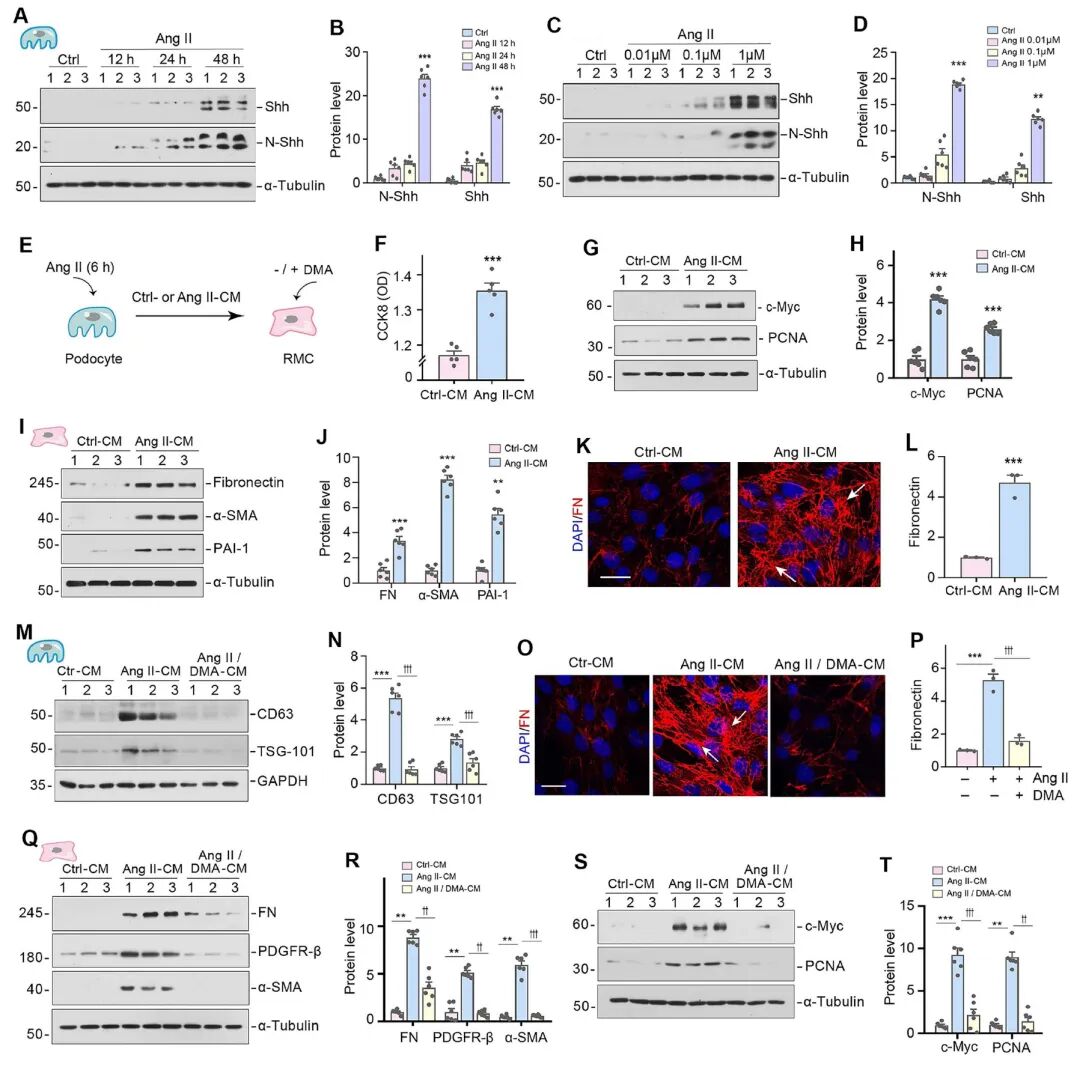
体外实验表明,使用药物Dimethyl Amiloride(DMA)抑制足细胞的EVs分泌后,由足细胞条件培养基诱导的系膜细胞活化(FN, α-SMA, PDGFR-β表达)和增殖(c-Myc, PCNA表达)被显著抑制。这证明EVs是足细胞-系膜细胞通讯所必需的。
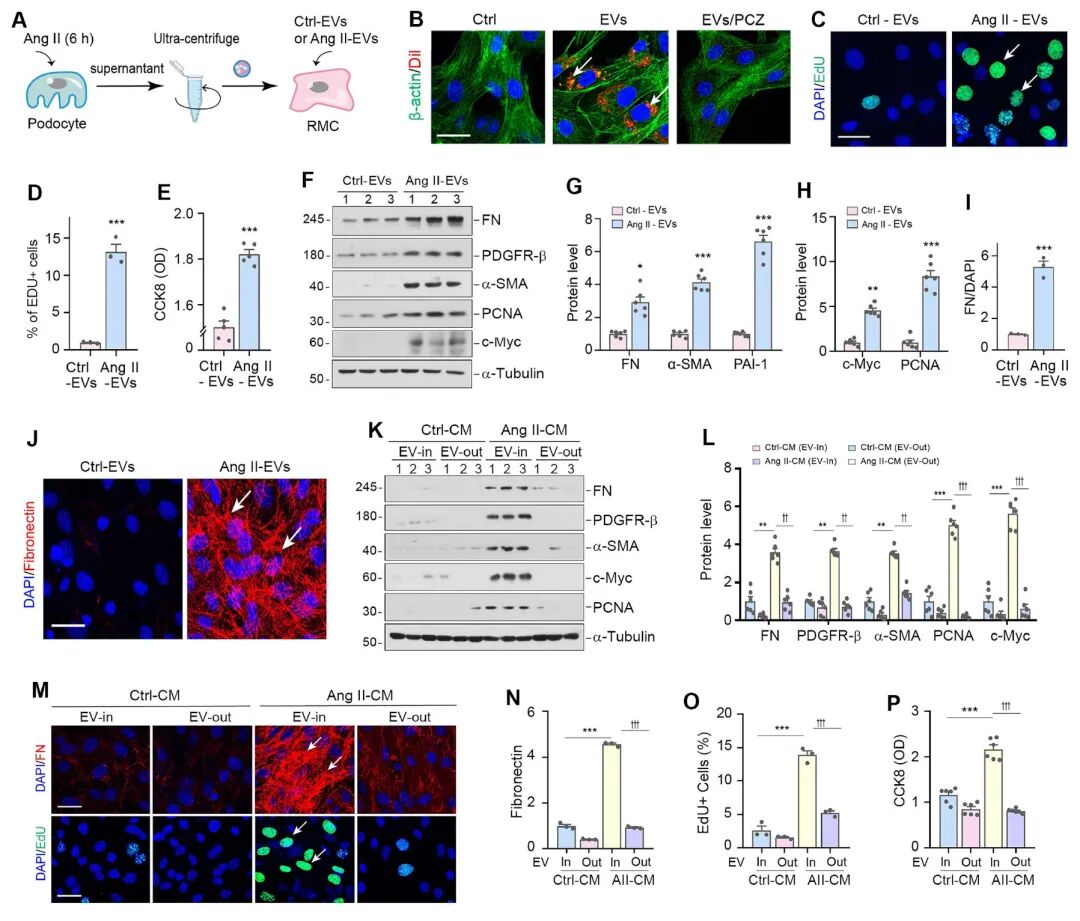
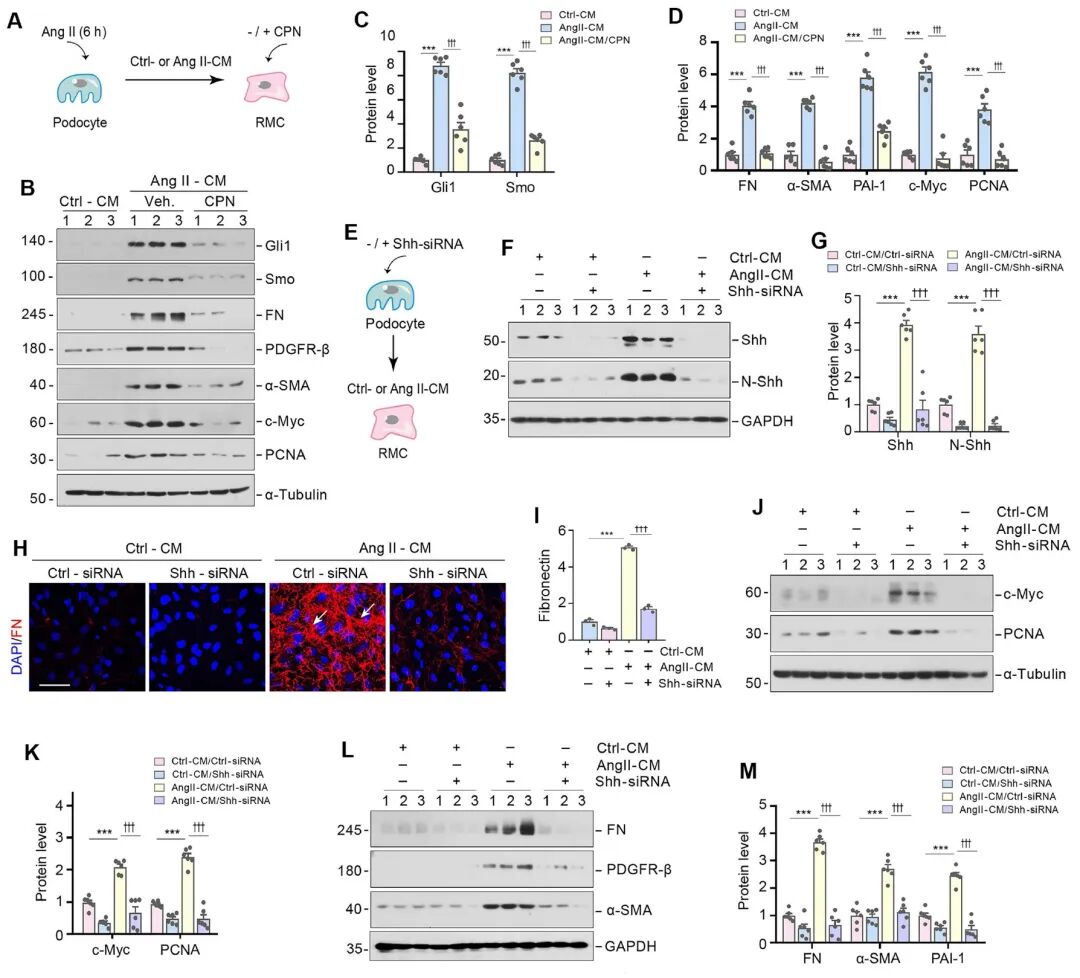
将Ang II-EVs与系膜细胞共培养,能显著促进后者的活化、增殖及ECM沉积。若使用Shh siRNA敲低足细胞中的Shh表达,或使用抑制剂Cyclopamine(CPN)阻断系膜细胞的Shh信号通路,则Ang II-EVs的激活效应被取消。这直接证明了EVs中的Shh是介导这一过程的关键因子。
在Ang II/ADR诱导的小鼠肾小球疾病模型中,静脉注射Ang II-EVs会加重肾小球硬化,而同时使用CPN抑制Shh信号则可逆转这种加重效应。反之,使用DMA抑制体内EVs的分泌,则能显著改善模型小鼠的肾小球硬化病变。
本研究阐明了足细胞损伤通过释放富含Shh信号通路的EVs,激活系膜细胞并导致肾小球硬化的新机制。RayBiotech抗体芯片(货号:AAM-CYT-G2000,一次性检测小鼠样本中144种细胞因子)在该研究中起到了关键性的发现作用,通过高通量筛选精准地鉴定出N-Shh是损伤足细胞EVs中最主要的差异蛋白,为整个研究指明了Shh信号通路这一核心方向。该研究不仅揭示了蛋白尿向肾小球硬化进展的细胞间通讯机制,也提示靶向EVs或其携带的Shh可能是治疗肾小球疾病的新策略。
文章亮点
关键技术:借助RayBiotech小鼠细胞因子抗体芯片(G2000) 筛选144种因子,精准锁定N-Shh为损伤足细胞囊泡中的关键效应分子;
突破性发现:阐明Shh通过囊泡“包裹”传递至系膜细胞,驱动其活化与增殖,连接蛋白尿与肾小球硬化两大病理过程;
治疗新靶点:抑制囊泡释放或阻断Shh信号可显著缓解肾小球病变,为临床干预提供新策略。
点击全文,了解细胞外囊泡如何成为肾病进展的“信号快递员”!