瑞博奥(广州)生物科技股份有限公司
16 年
手机商铺
- NaN
- 0
- 0
- 2
- 2
推荐产品
技术资料/正文
机器学习获得诺贝尔物理学奖,辅助流行病学研究快速锁定关键靶标
76 人阅读发布时间:2025-03-17 16:05
10月8日,瑞典皇家科学院宣布,将2024年诺贝尔物理学奖授予美国科学家约翰·霍普菲尔德和英裔加拿大科学家杰弗里·辛顿,以表彰他们通过人工神经网络实现机器学习而作出的奠定性发现和发明。

趁着诺奖的风波,未来机器学习的应用必将迎来应用及发文的大爆发,
尤其是在医学研究领域,在疾病标志物及关键因素的锁定上,有机器学习辅助必定犹如神助!
RayBio精准多因子检测试剂盒,单次实验单个样本可检测几百上千个微量功能性细胞因子表达,在疾病大队列研究中,结合机器学习方法学的建立高效、快速锁定疾病机制关键靶标,药物作用靶标,大大提升临床转化效率。
杂志名称:Scientific Reports
文章题目:Osteoarthritis of the Temporomandibular Joint can be diagnosed earlier using biomarkers and machine learning
第一作者:Jonas Bianchi
通讯作者:Jonas Bianchi
单位:密歇根大学,圣保罗州立大学
本实验所用产品:定制人类定量抗体芯片
实验样品类型:唾液和血清
研究摘要 Abstract
骨关节炎(OA)影响全球数百万人,导致他们多年疼痛和残疾。随着年龄的增长,颞下颌关节骨关节炎(TMJ-OA)会引起慢性残疾。颞下颌关节是研究OA早期骨变化的独特模型,因为关节骨表面仅被颞下颌关节髁中的一层薄薄的纤维软骨覆盖。TMJ-OA是一种多系统性疾病,涉及众多病理生理过程,需要全面评估进行性软骨退化、软骨下骨重塑和慢性疼痛的特征。
研究者希望在OA患者骨形态退化发生之前进行诊断并干预。于是建立了4个模型Logistic Regression, Random Forest, LightGBM, XGBoost,综合评估了52个临床、生物学和高分辨率CBCT(影像组学)标志物。建模的特征包括:是否头痛,张口无疼痛范围,Haralick相关性,熵和TGF-β1在唾液中的相互作用,血清中的VE-钙粘蛋白和唾液中的血管生成素等。结果表明,具有这些特征和交互作用的XGBoost + LightGBM模型在诊断TMJ-OA状态时准确率达到了0.823,AUC 0.870和F1得分0.823。因此,研究团队希望促进未来对骨关节炎患者特定治疗干预的研究,从而改善关节的健康。
研究结果
Part.
1
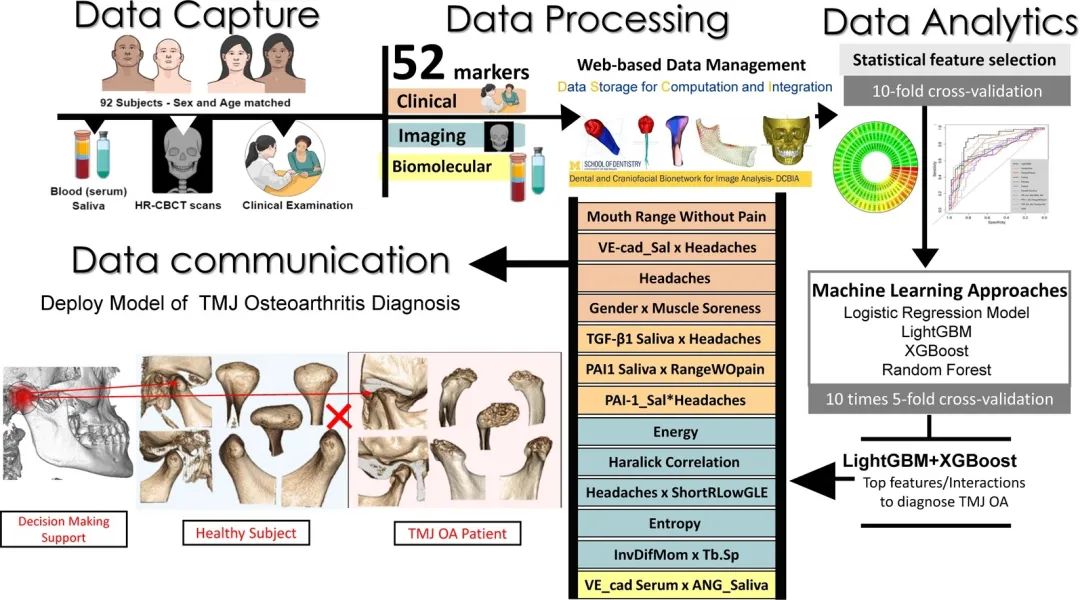
基于网络的平台,用于存储和计算临床、影像组学和生物分子标记的数据分析
用Data Storage for Computation and Integration (DSCI)存储和集成来自多个来源的患者信息进行数据管理。DCSI通过Data Base lnteractor插件与3D Slicer平台通信,允许用户上传临床,成像和生物标志物。
Part.
2
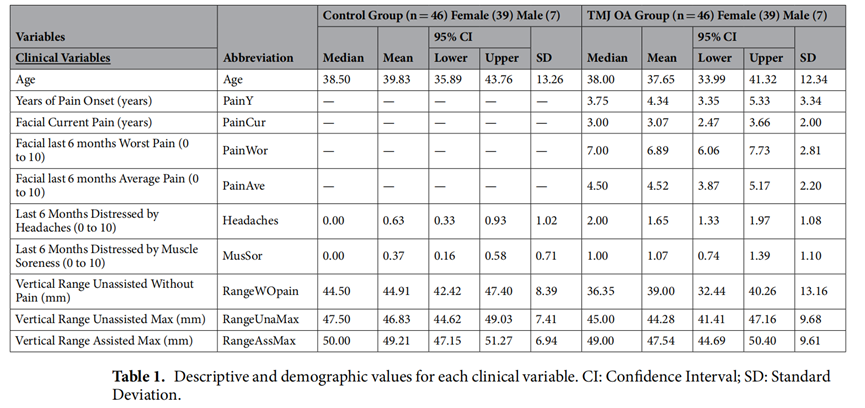
对照组和TMJ-OA患者组的放射学特征、生物学特征和影像学特征研究
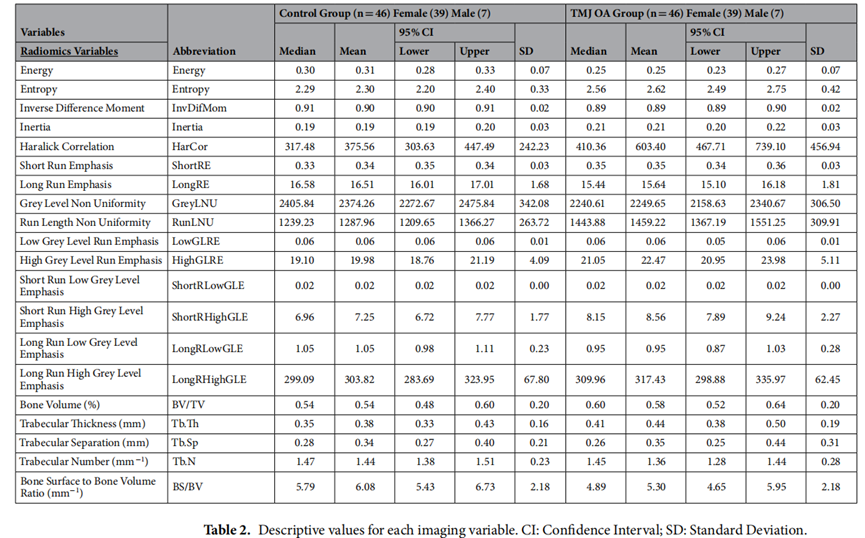
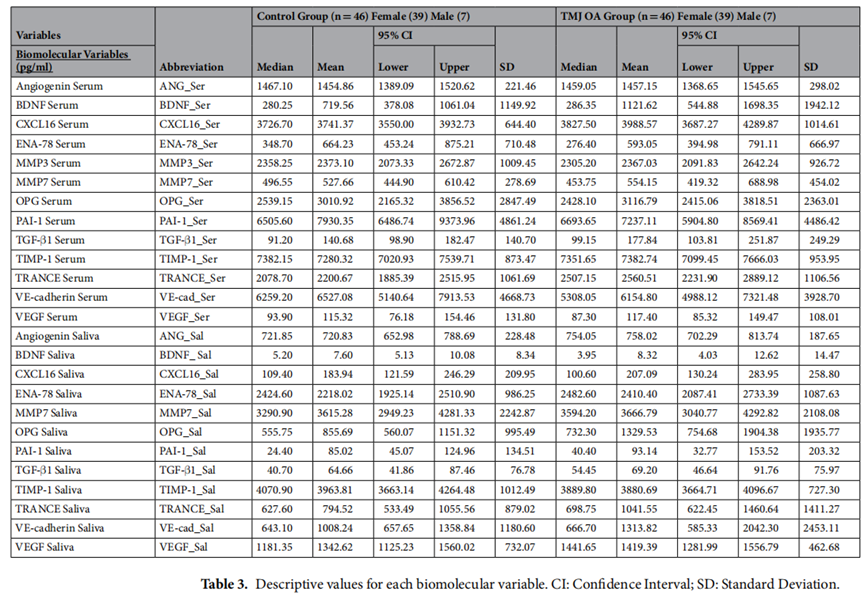
放射学特征主要集中在下颌髁小梁骨的初始形态变化(Table 2);生物学特征与颞下颌关节滑膜中检测到的VE-cad,ANG,TGF-β1和PAI-1与OA患者的髁突形态相关(RayBio 定制抗体芯片,Figure 2);影像学特征与疼痛相关或受疼痛限制相关(Table 3)。

Part.
3
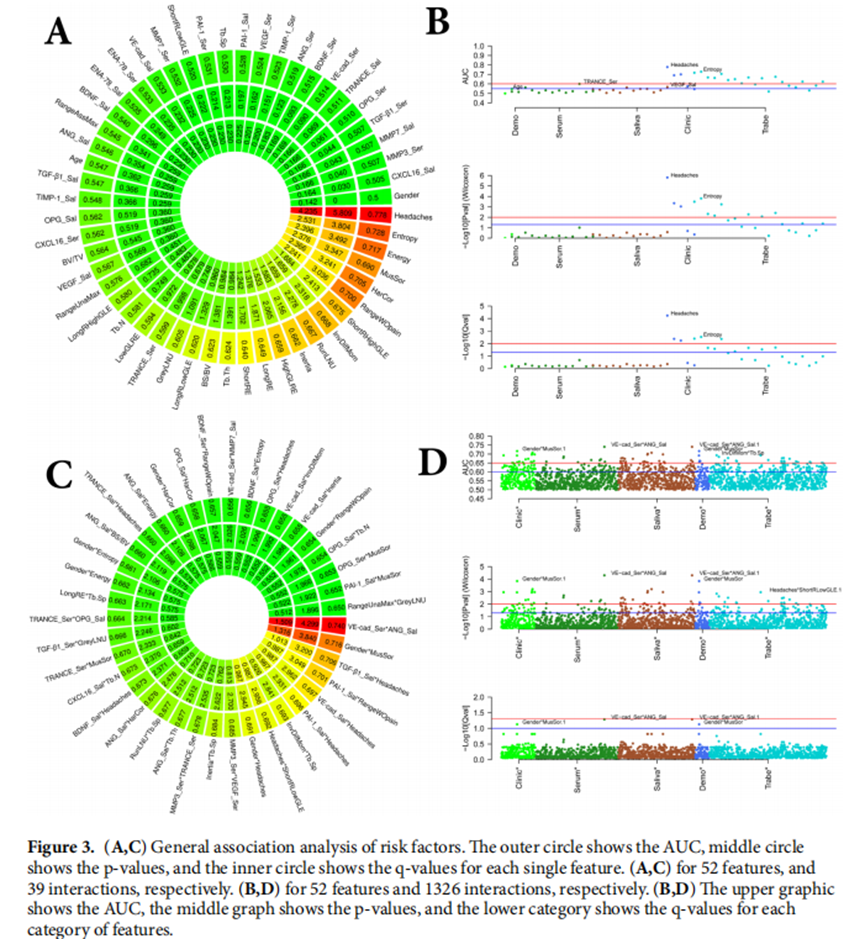
用上述特征进行TMJ-OA的特征选择和模型构建
Part.
4
主要特征和交互特征诊断TMJ-OA
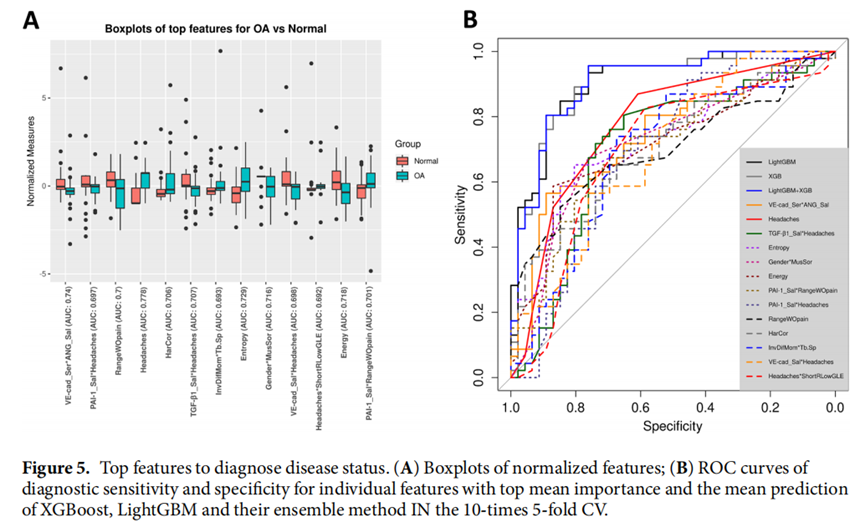
研究结论 Conclusion
总之,深入统计学习分析是基于52个单独特征和多个交互特征综合分析。研究人员筛选了每个特征的诊断性能(图3-5),并根据最相关的蛋白、临床、影像学特征构建了机器学习模型。研究人员的最终预测模型使用LightGBM + XGBoost预测TMJ-OA状态的准确率为0.823(SD:0.029),具有1378个特征交互作用。重要的是,研究团队展示了新工具、数据采集、管理和方法的全面整合,以改善关节健康并预测患者特定的TMJ-OA状态。