瑞博奥(广州)生物科技股份有限公司
16 年
手机商铺
- NaN
- 0
- 0
- 2
- 2
推荐产品
技术资料/正文
IF12.4| RayBio大鼠高通量芯片助力揭示3D心肌组织改善心脏功能新机制
197 人阅读发布时间:2025-03-17 14:42
缺血性卒中是导致成人神经功能障碍的常见原因,尽管在急性溶栓治疗和随后的神经康复训练方面取得了进展,但其治疗仍然面临挑战。卒中后,大脑皮质网络可能发生重构,导致皮质兴奋性异常增高,这种兴奋性增高与神经功能的恢复密切相关。因此,寻找能有效调节卒中后皮质兴奋性的治疗方法至关重要。
近年来,间充质干细胞(MSCs)因其具有多向分化潜能和免疫调节特性,在神经退行性疾病和损伤的治疗中展现出巨大潜力。其中,人骨髓来源的间充质干细胞(hMSCs)经过特定修饰后(如SB623细胞),在临床前和临床试验中已被用于治疗创伤性脑损伤和脑缺血卒中后的慢性运动障碍。然而,这些细胞治疗的确切机制尚不清楚。
美国加利福尼亚大学研究团队通过在大鼠中风后慢性阶段移植hMSC-SB623细胞,探讨了其对皮质兴奋性和神经修复的影响,发现该细胞能显著纠正皮质过度兴奋性,促进神经再生和突触可塑性,并改善全身免疫反应。
研究思路
本研究旨在探讨hMSC-SB623细胞治疗对缺血性中风后慢性阶段大鼠模型的皮质网络兴奋性、脑组织和外周血液的影响。研究采用光凝法诱导大鼠右感觉运动皮质的局灶性缺血性中风,术后1个月将hMSC-SB623细胞或对照溶液注射到中风周边皮质。术后1周开始进行体外电生理学检测,评估皮质兴奋性。同时,对脑组织进行组织学分析,检测与神经再生、突触和细胞可塑性相关的因子变化,并通过全血RNA测序和血清蛋白分析(RayBio Rat L1500芯片)评估外周血液的变化。

术前状态:中风后,大鼠皮质的兴奋性显著增加,表现为对白质刺激的反应增强,这种过度兴奋性主要集中在皮质第4层。
hMSC-SB623细胞治疗效果:hMSC-SB623细胞移植后,中风诱导的皮质过度兴奋性被显著降低,皮质兴奋性恢复至对照水平。例如,在白质刺激下,中风组的皮质第4层的突触前和突触后反应均显著增强,而hMSC-SB623细胞移植后,这些反应被显著抑制,突触前反应的幅度和面积在大多数刺激强度下均被归一化。
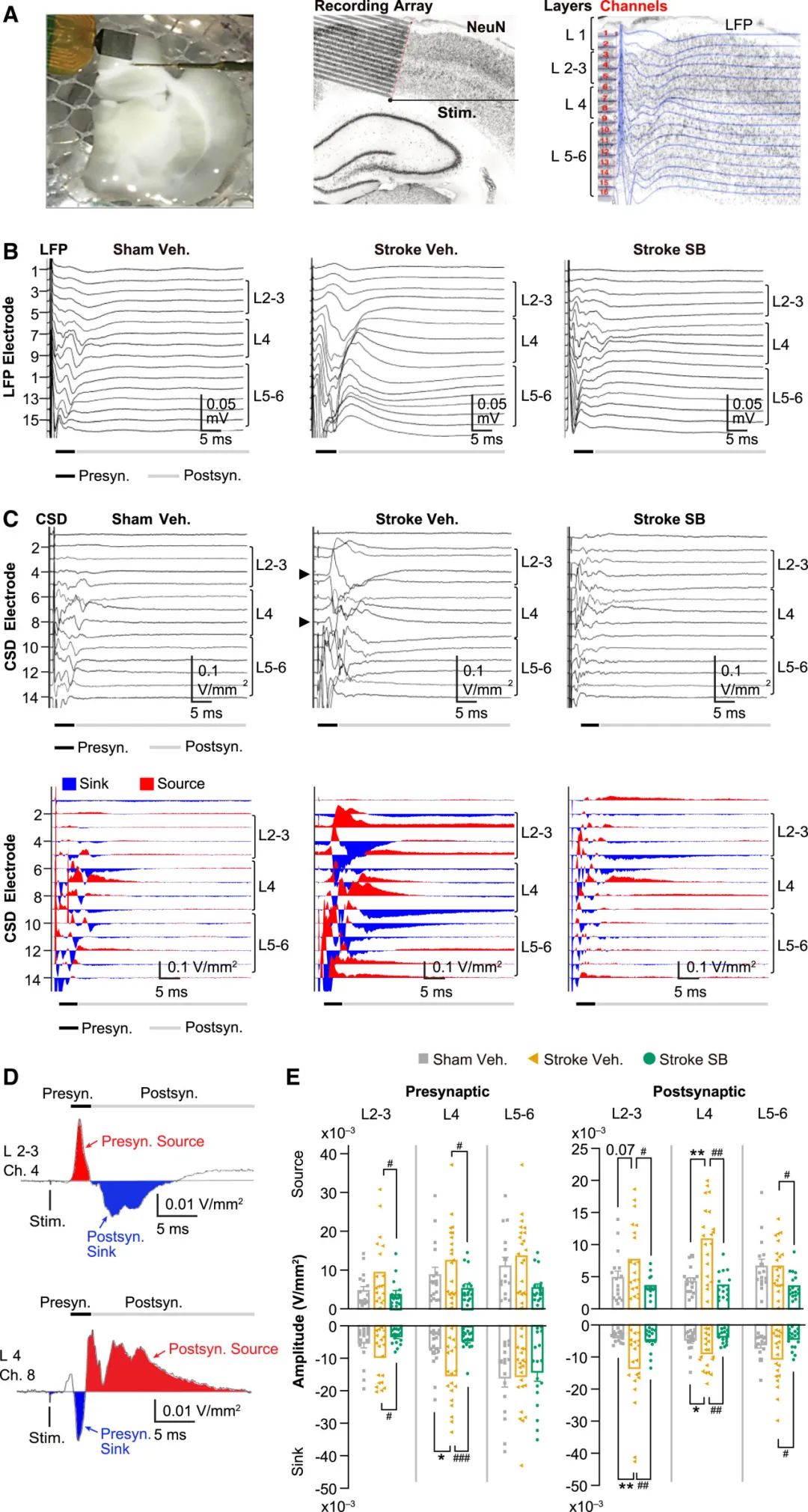
fig.2
细胞存活情况:移植后7天,存活的hMSC-SB623细胞数量较少,仅占注射剂量的0.18%,但这些细胞在皮质和皮层下区域均有分布,甚至在对侧半球的胼胝体中也有发现。
脑组织变化
神经元和脑组织体积:中风导致皮质神经元和脑组织显著丢失,但hMSC-SB623细胞治疗并未显著影响脑组织体积或神经元数量。
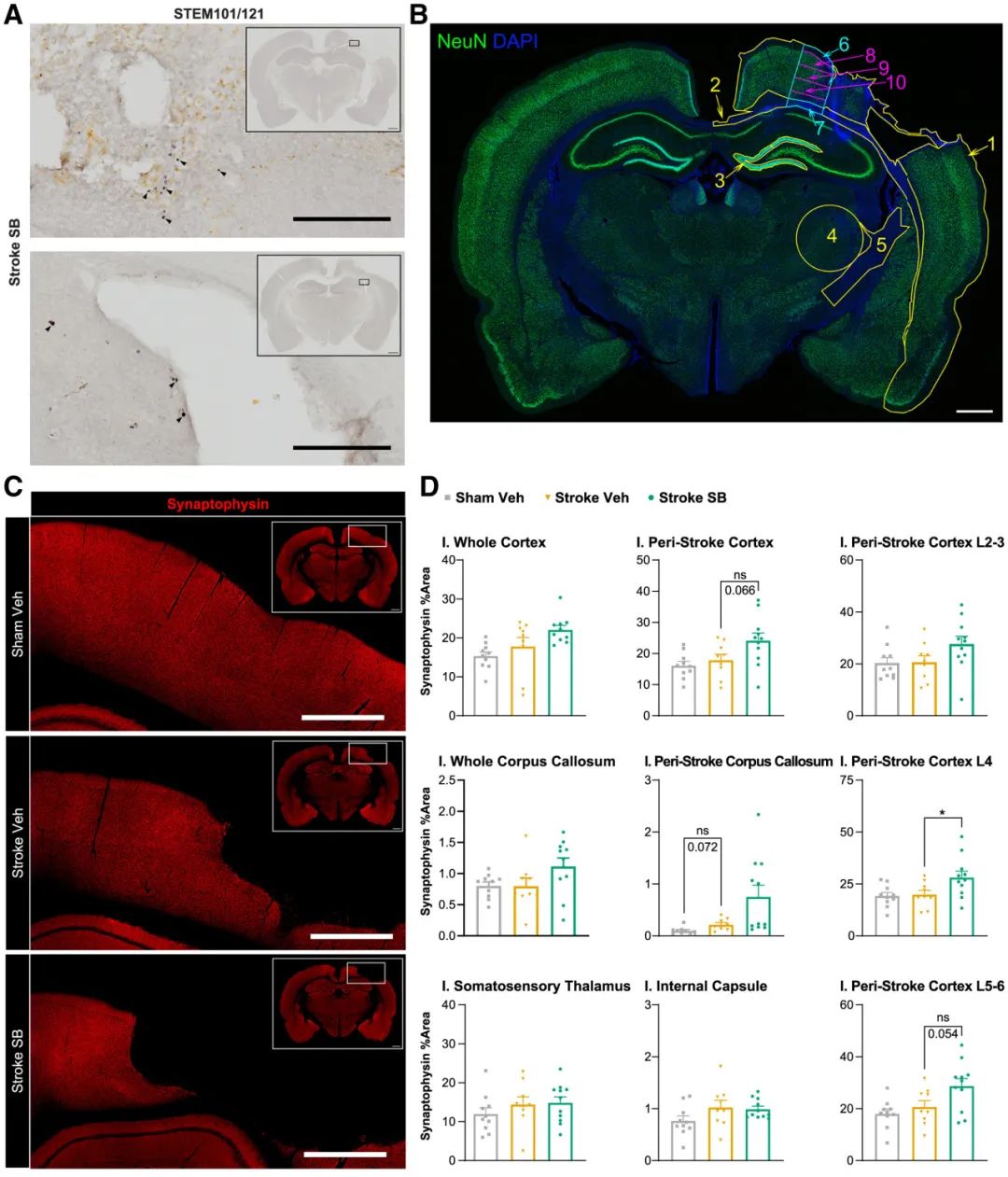
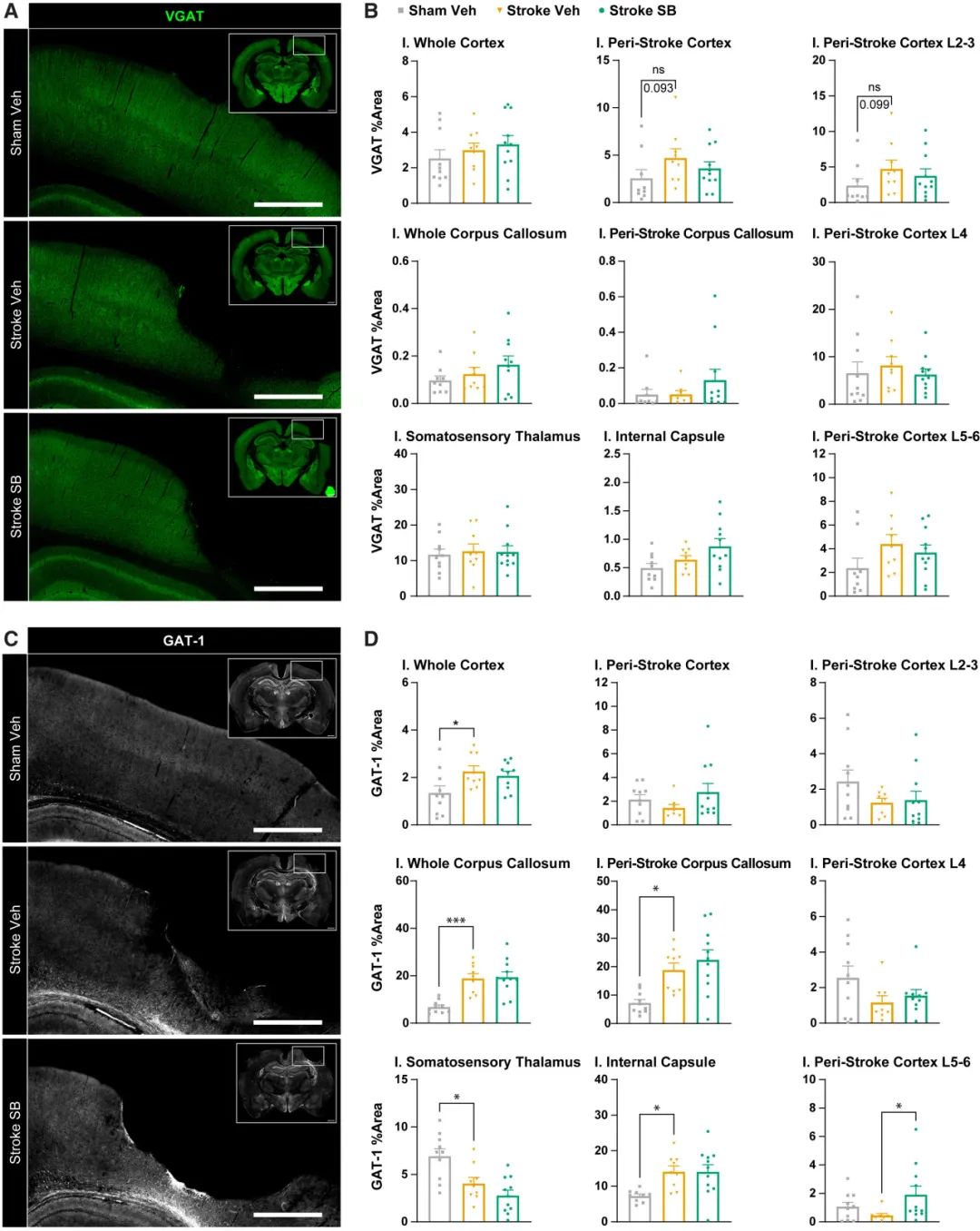
突触和细胞可塑性相关因子:hMSC-SB623细胞治疗显著增加了突触素(synaptophysin)的表达,特别是在皮质第4层,表明可能通过促进突触生成或增强突触可塑性来改善皮质兴奋性。此外,hMSC-SB623细胞治疗还增加了GABA重摄取转运蛋白GAT-1在皮质第5和6层的表达,可能通过调节GABA的可用性来影响皮质兴奋性。
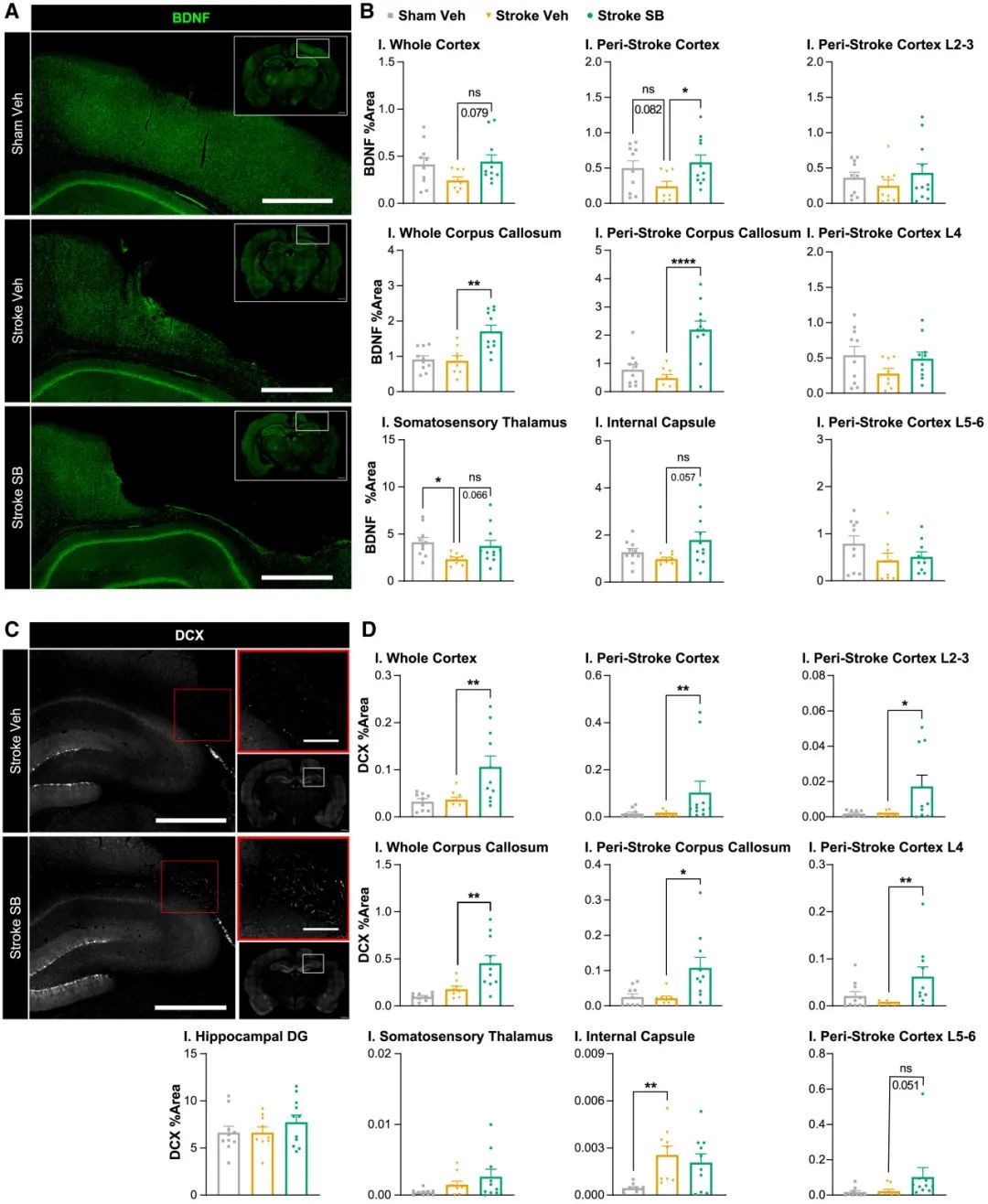
神经营养因子:hMSC-SB623细胞治疗显著增加了脑源性神经营养因子(BDNF)在皮质和胼胝体的表达(fig.4),BDNF已知可刺激GAT-1介导的GABA运输,可能通过促进突触可塑性和髓鞘修复来改善神经功能。
神经干细胞和少突胶质细胞:hMSC-SB623细胞治疗增加了双皮质素(DCX)阳性神经干细胞和少突胶质细胞前体细胞(OPCs)的增殖,表明可能通过促进神经再生和髓鞘修复来改善神经功能。
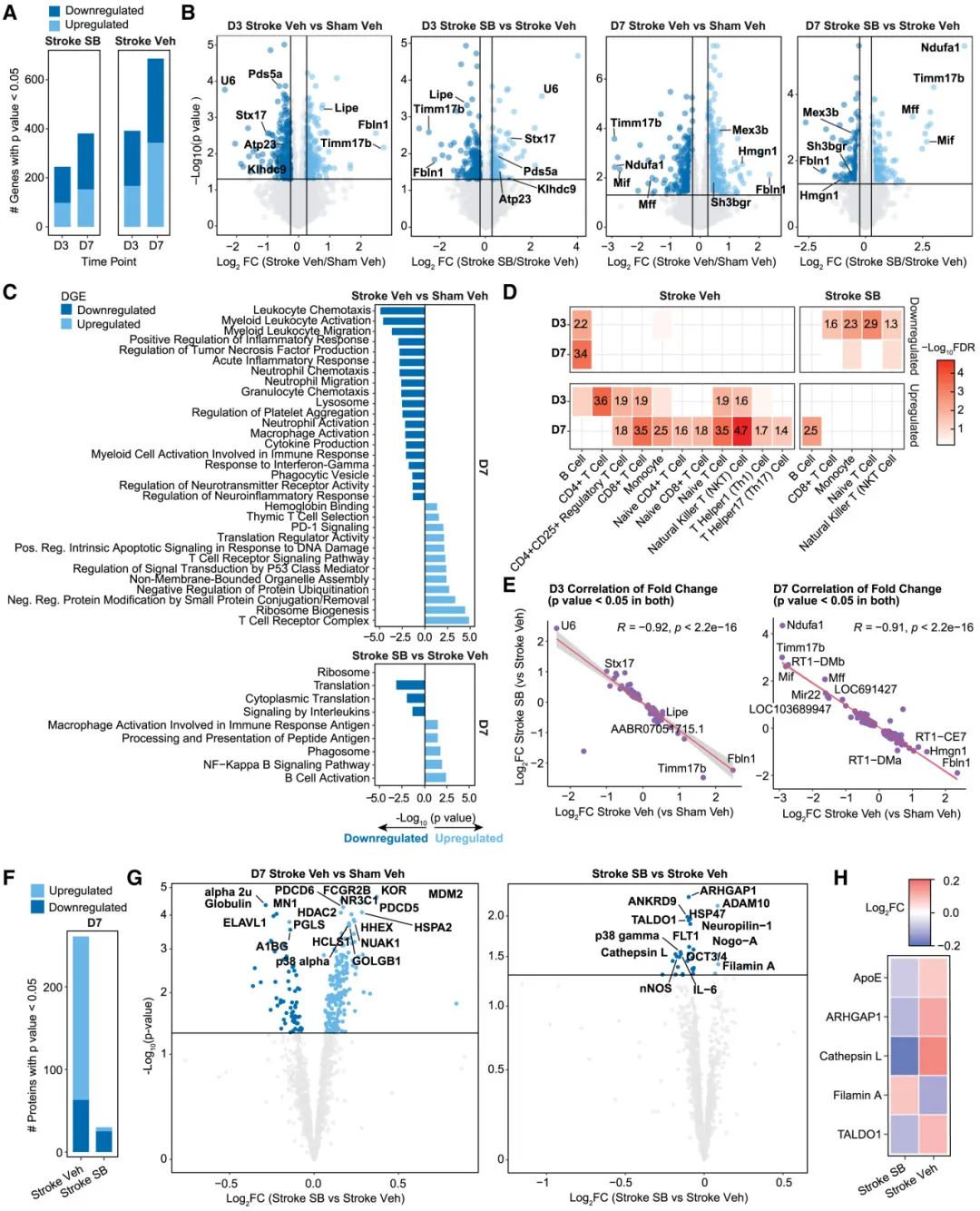
基因表达:中风和hMSC-SB6223细胞治疗均对大鼠外周血液基因表达产生显著影响,hMSC-SB623细胞治疗可逆转中风诱导的外周血液基因表达变化,例如CD8b基因表达在中风后下调,而hMSC-SB623细胞治疗后下调趋势被抑制。
蛋白表达:中风后血清中多种蛋白表达发生显著变化,通过蛋白芯片(RayBio AAR-BLG-1500)分析发现,hMSC-SB623细胞治疗可逆转部分中风诱导的血清蛋白水平变化,例如filamin A、cathepsin L、ApoE等蛋白的表达水平在中风后发生改变,而hMSC-SB623细胞治疗后这些蛋白的表达水平被部分恢复。