瑞博奥(广州)生物科技股份有限公司
16 年
手机商铺
- NaN
- 0
- 0
- 2
- 2
推荐产品
公司新闻/正文
抗体芯片技术解码肿瘤微环境:如何发现治疗耐药的关键细胞因子网络
86 人阅读发布时间:2026-04-27 11:38
杂志名称:Drug Resistance Updates
影响因子:21.7
文章题目:Mechanisms of therapy resistance in the tumor microenvironment: Insights from antibody array–based cytokine profiling
肿瘤微环境中治疗耐药的机制:来自抗体芯片的解析
作者:Rochelle Wickramasekara,Valerie Jones,赵亚婷,罗树红(RayBiotech首席科学家)
通讯作者:孙国贵, 黄若磐(RayBiotech创始人)
单位:RayBiotech Life Inc., ;华北理工大学附属医院

研究背景
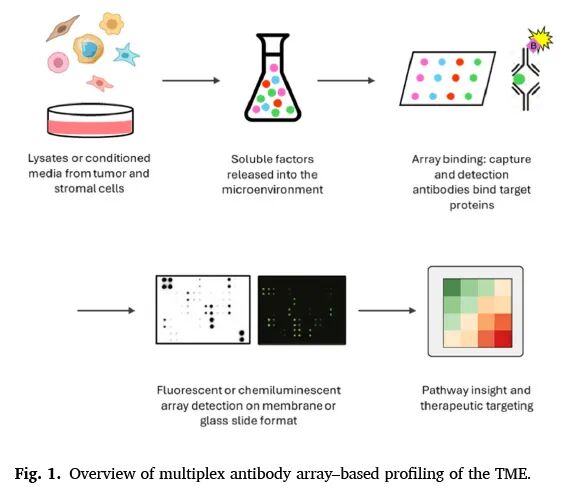
治疗耐药是实体瘤治疗失败和癌症相关死亡的主要原因。虽然肿瘤细胞内在的耐药机制已被广泛研究,但肿瘤微环境通过非遗传、细胞外信号传导方式在驱动治疗耐药中的作用日益受到重视。肿瘤微环境中的基质细胞和免疫细胞——包括成纤维细胞、巨噬细胞、内皮细胞和调节性免疫细胞——通过细胞因子信号传导、直接接触和细胞外基质重塑与肿瘤细胞相互作用,促进其存活、免疫逃逸和治疗适应性改变。本研究旨在系统综述基于抗体芯片的多重蛋白组学技术如何揭示肿瘤微环境中细胞因子介导的耐药机制,并探讨这些发现对化疗、靶向治疗、放疗和免疫耐药的临床意义。
1、相关成纤维细胞的异质性与细胞因子介导的耐药机制
通过抗体芯片技术对不同CAF亚群进行分泌组学分析,发现CAF存在显著的功能异质性。
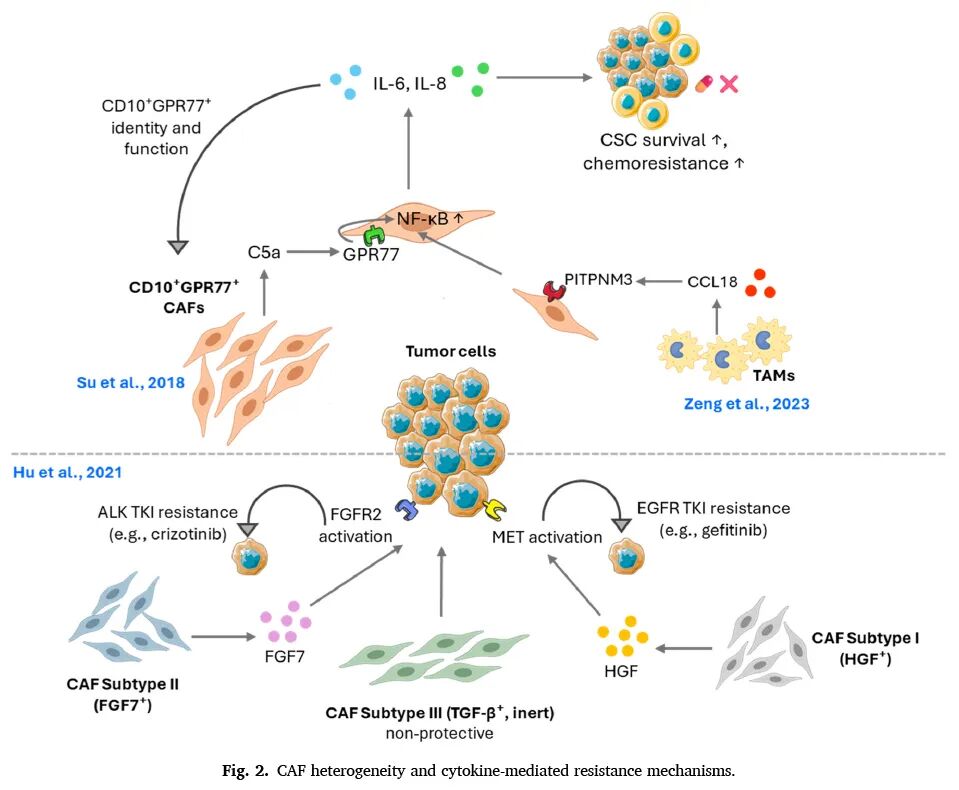
一项乳腺癌研究中,CD10⁺GPR77⁺炎症性CAF亚群高表达IL-6和IL-8,通过持续激活NF-κB信号维持肿瘤干细胞特性,导致化疗耐药。进一步研究发现,这一CAF亚群由TAM来源的趋化因子CCL18通过PITPNM3-NF-κB轴诱导形成,揭示了TAM-CAF-肿瘤细胞间的细胞因子调控网络。在非小细胞肺癌中,通过抗体芯片鉴定出三种功能不同的CAF亚型:亚型I分泌HGF,通过MET信号导致EGFR抑制剂耐药;亚型II分泌FGF7,通过FGFR2信号导致ALK抑制剂耐药;亚型III则高表达TGF-β,不具有耐药促进作用。
2、CAF通过多样化的细胞因子信号网络驱动多模式治疗耐药,主要特征包括:
①信号汇聚性:不同细胞因子(IL-6、IL-8、IL-11、HGF、IGF1、PAI-1、CXCL1等)汇聚于有限的下游通路(STAT3、AKT、ERK、NF-κB)
②通路协同性:耐药表型常需多个信号通路协同激活,而非单一因子驱动
③治疗压力诱导可塑性:化疗、放疗、靶向治疗可重塑CAF表型,增强其促耐药功能
④免疫调节功能:CAF通过PD-L1非经典功能和细胞因子分泌调控免疫微环境,介导免疫治疗耐药
⑤功能异质性:不同CAF亚群具有独特的细胞因子分泌谱和耐药介导能力
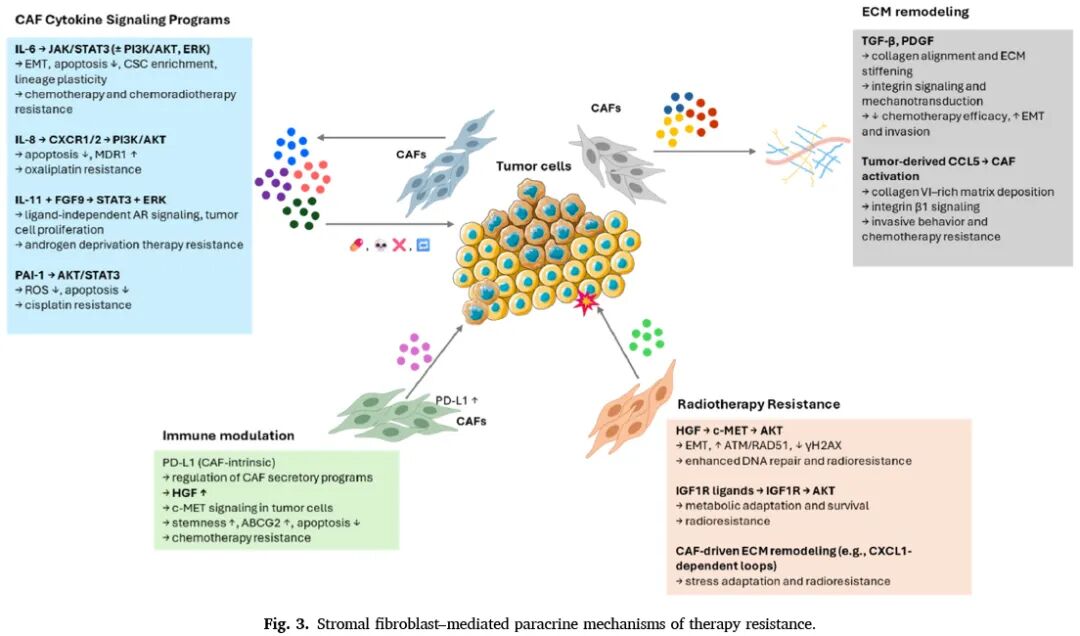
3、TAM和髓系细胞通过多样化的细胞因子信号网络驱动多模式治疗耐药,主要特征包括:
①信号网络复杂性,肿瘤细胞通过Galectin-9/Tim-3、IL-34/CSF-1R、CCL2/CCR2等轴重塑TAM表型;TAM通过CCL15/CCR1、IL-6家族/gp130等轴赋予肿瘤细胞治疗耐受性
②反馈环路稳定性,TAZ-IL-34-TGF-β1等自我维持的旁分泌环路将肿瘤锁入巨噬细胞主导、治疗抵抗的微环境状态
③治疗模式普适性,髓系细胞介导的耐药跨越免疫治疗(抗PD-1/PD-L1)、靶向治疗(吉非替尼)和化疗(长春新碱)
④受体非依赖性激活,髓母细胞瘤中gp130-STAT3通路的激活不依赖于经典IL-6受体表达,体现了信号通路的适应性
⑤肿瘤固有程序驱动,肿瘤细胞内在的遗传改变(PTEN缺失、NRAS突变)和转录程序(ZBTB18、H19-IRP、TAZ)直接决定髓系环境的免疫抑制程度和治疗反应
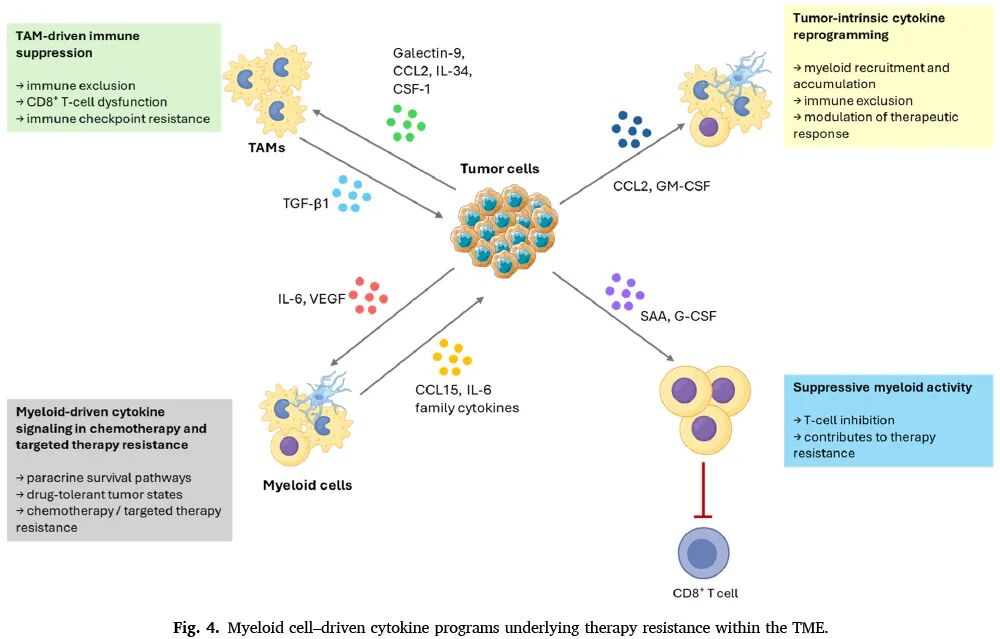
4、调节性免疫细胞介导的免疫抑制
在胃癌中,转录因子ZFP64上调galectin-1表达;肿瘤来源的GAL-1直接抑制CD8⁺T细胞功能,同时激活肿瘤固有MAPK和PI3K-AKT信号,促进干细胞样表型和化疗耐药。在口腔鳞癌中,突变p53改变趋化因子和细胞因子表达谱,抑制CD8⁺T细胞募集信号,增强IL-10和TGF-β等免疫抑制因子,导致PD-1和TIGIT阻断耐药。在食管鳞癌中,新辅助放化疗后反应不良的肿瘤保留CCR4/CCR6相关趋化因子信号,伴随调节性免疫细胞富集和持续T细胞功能障碍。
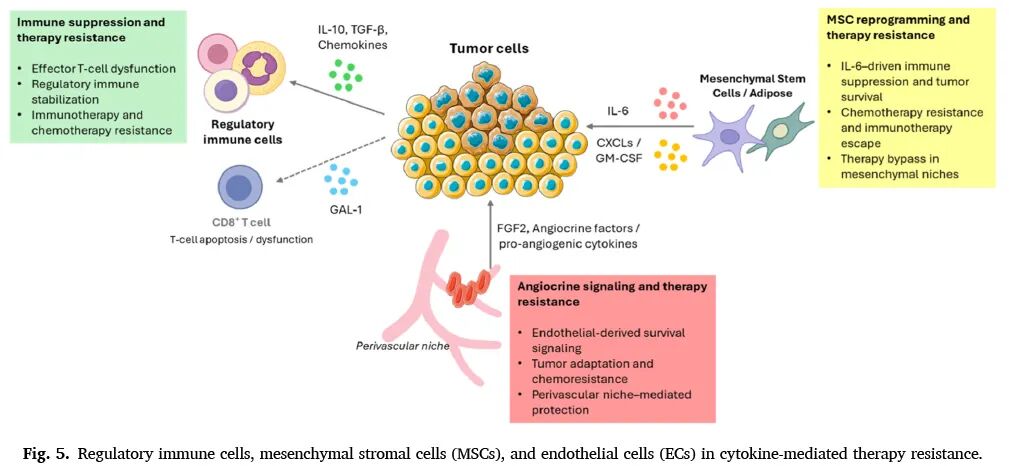
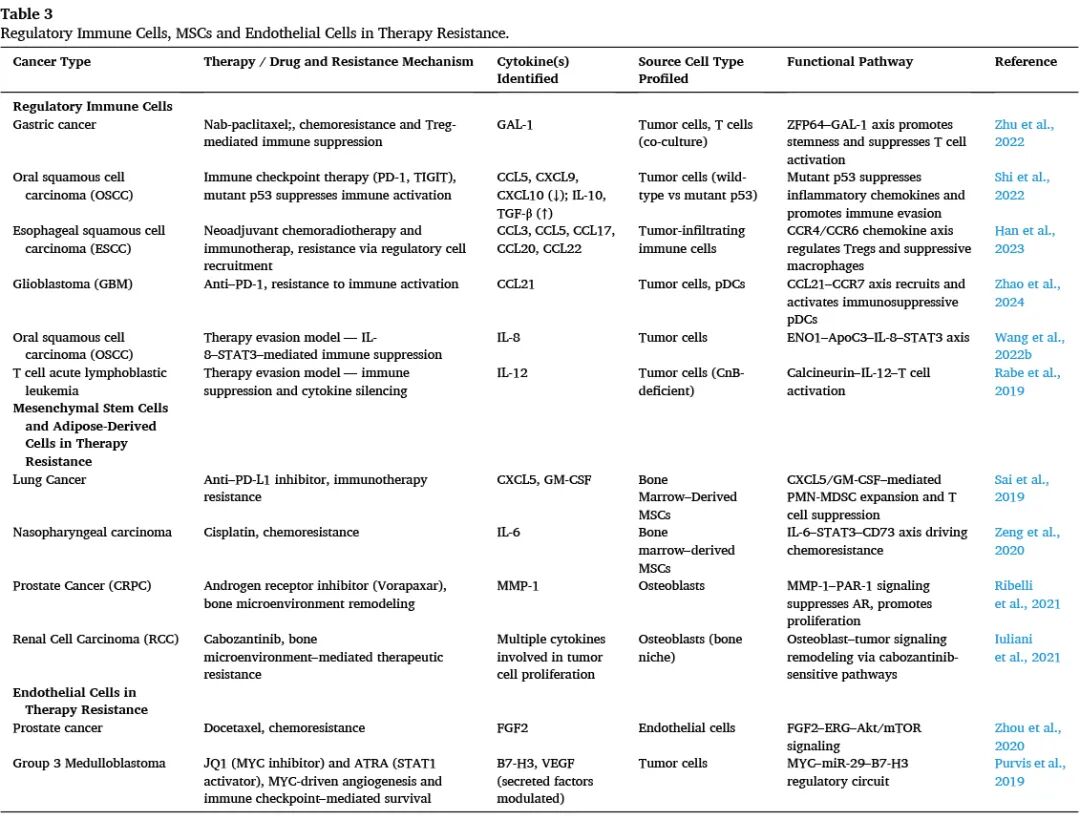
5、间充质干细胞和内皮细胞介导的耐药
在肺癌模型中,肿瘤驯化的骨髓MSC分泌CXCL5和GM-CSF,驱动PMN-MDSC扩增和动员,损害细胞毒性T细胞功能,导致抗PD-L1治疗耐药。在鼻咽癌中,MSC来源的IL-6通过STAT3信号上调肿瘤细胞CD73表达,促进顺铂耐药。在内皮细胞介导的耐药研究中,内皮细胞来源的FGF2通过诱导ERG表达和激活Akt/mTOR信号,导致前列腺癌多西他赛耐药。
6、临床靶向细胞因子通路的转化研究
临床研究显示,靶向IL-6/STAT3信号在免疫治疗耐药患者中仅在具有炎症或基质富集TME特征的亚组中观察到疗效。HGF/MET通路靶向在未经选择的人群中疗效有限,但在HPV阴性或c-MET过表达的生物标志物定义亚组中显示获益。CSF1/CSF1R和CXCR2靶向虽能有效重塑髓系 compartment,但单一靶向不足以克服既有免疫耐药。CXCL12/CXCR4靶向在胰腺癌中通过破坏CAF介导的趋化因子屏障,恢复T细胞浸润,在免疫排除型肿瘤中显示出治疗潜力。
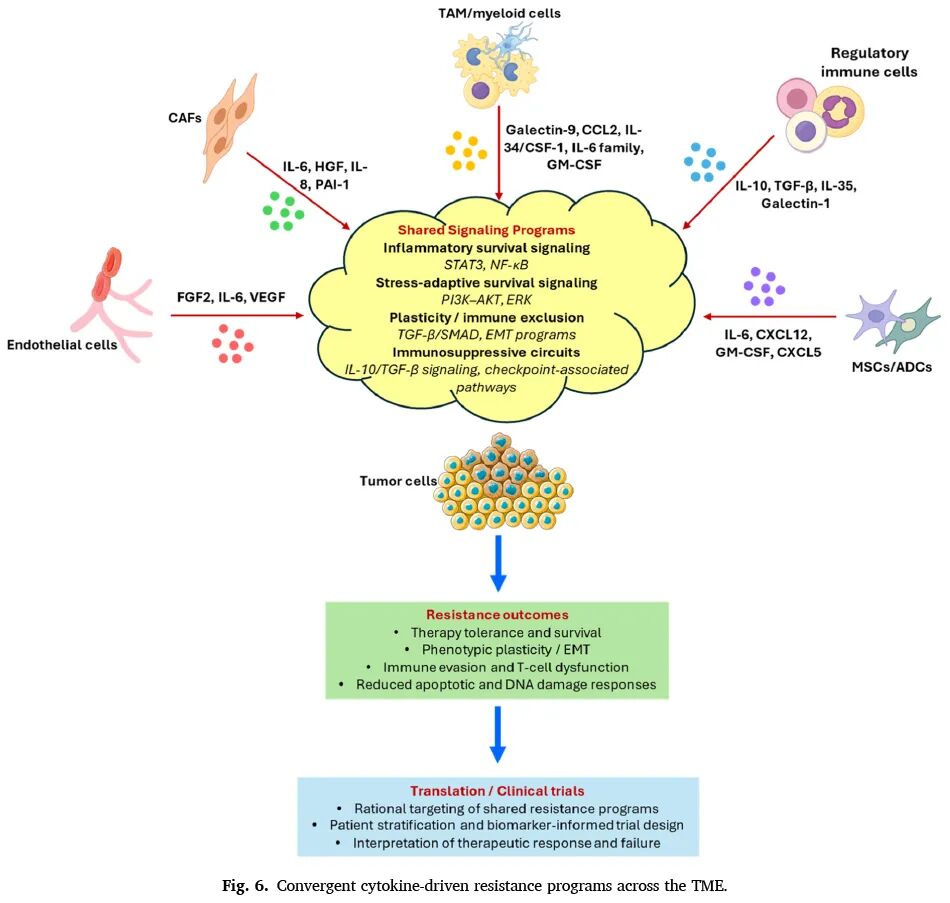
结论
本综述系统总结了基于抗体芯片的多重蛋白组学技术在揭示肿瘤微环境中介导治疗耐药的细胞因子信号网络中的应用。研究发现,肿瘤相关成纤维细胞、肿瘤相关巨噬细胞、调节性免疫细胞、间充质干细胞和内皮细胞通过分泌多种细胞因子和趋化因子,形成复杂的旁分泌和自分泌信号网络,激活STAT3、NF-κB、PI3K/AKT、MAPK和TGF-β/SMAD等共享信号通路,共同驱动肿瘤细胞存活、免疫逃逸、表型可塑性和治疗适应。尽管细胞因子来源各异,但这些信号汇聚于有限的共享通路,最终导致化疗、靶向治疗、放疗和免疫治疗的耐药表型。临床靶向研究进一步表明,细胞因子通路的治疗干预效果取决于生物学背景、通路冗余性和患者分层,强调了多重蛋白组学分析在识别耐药相关信号通路和指导精准治疗策略中的价值。